![]()

文章信息
期刊:American Journal of Respiratory and Critical Care Medicine
影响因子(IF):16.494
文章名称:Is PKM2 Phosphorylation Prerequisite for Oligomer Disassembly in Pulmonary Arterial Hypertension?
(点击获取全文)
作者:Novoyatleva T等
作者单位:德国吉森大学
研究背景
肺动脉高压(PAH)是一种不可治愈的血管疾病,由于肺部血管重构以及肺部血管阻力增加,最终导致右心衰竭甚至死亡(1)。PAH与癌症的主要病理生理机制相同,包括大量的代谢重编程,使用糖酵解途径取代线粒体的氧化磷酸化获取能量(WarBurg效应)。丙酮酸激酶(PK)负责催化糖酵解途径的最后一步反应,即将磷酸烯醇式丙酮酸(PEP)上的磷酸根转移到ADP上,从而产生丙酮酸(Pyruvate)和ATP。肌肉型丙酮酸激酶基因(PKM)选择性剪接产生PKM1和PKM2两种同工酶,PKM1在分化终末组织中产生组成型活性四聚体,PKM2在增殖细胞和肿瘤中形成高活性的四聚体以及低活性二聚体/单体(2)。多种变构效应物(如fructose-1,6-bisphosphate)及翻译后修饰(Y105 及 S37的磷酸化)控制PKM2构象变化来变实现单体、二聚体和四聚体的动态平衡。PKM2从四聚体转变成低活性二聚体/单体,最终将糖酵解途径转向生物合成途径中,促进Warburg效应。因此,PKM2低聚反应是决定酶的最终活性的关键因素,造成代谢重编程。Erk1/2(由生长因子激活)依赖型磷酸化导致PKM2核转运进而激活代谢基因的转录活性(3)。此外,核PKM2作为异链菌素(β-catenin)的共活化剂诱导细胞周期蛋白D1和c-myc(Cyclin D1和c-Myc)表达,突出PKM2对细胞周期进程的非代谢作用(4)。聚ADP核糖聚合酶-1(PARP-1)信号通路调节核PKM2功能,在PAH发展中发挥着至关重要的作用(5,6)。
各种癌症类型的血浆中二聚体PKM2含量均有提高(2),表明PKM2可作为代表细胞代谢活性和增殖能力的非器官特异性生物标记物。此外,最近的研究表明,在肺动脉高压(PH)内皮细胞和成纤维细胞中,PKM2的代谢和增殖异常(7,8)。PH中PKM2的血浆水平及PAH中PKM2的表达、定位、磷酸化以及寡聚化程度在很大程度上仍然是未知的。
研究结果
为了研究循环PKM2是否是PH的标志物,作者分析了从Giessen肺高血压登记处获得的多种病因的患者血浆。(ethics approval no. 186/16,266/11)(9)。来自健康志愿者的外周血浆和来自平均肺动脉压力<25mmHg(非PH)个体的中心静脉血浆作为非PH对照。与健康对照(n=30)、非PH对照(n=31)和慢性血栓栓塞PH患者(IV组PH;n=38)相比,血浆中二聚体PKM2的水平在特发性PAH(IPAH;n=35)患者中显著降低(图1A)。受试者工作特征(ROC)分析以PKM2区分IPAH患者与非PH对照的可行性,结果显示血浆PKM2与血流动力学参数、患者患病的严重程度和生存并无关联性。
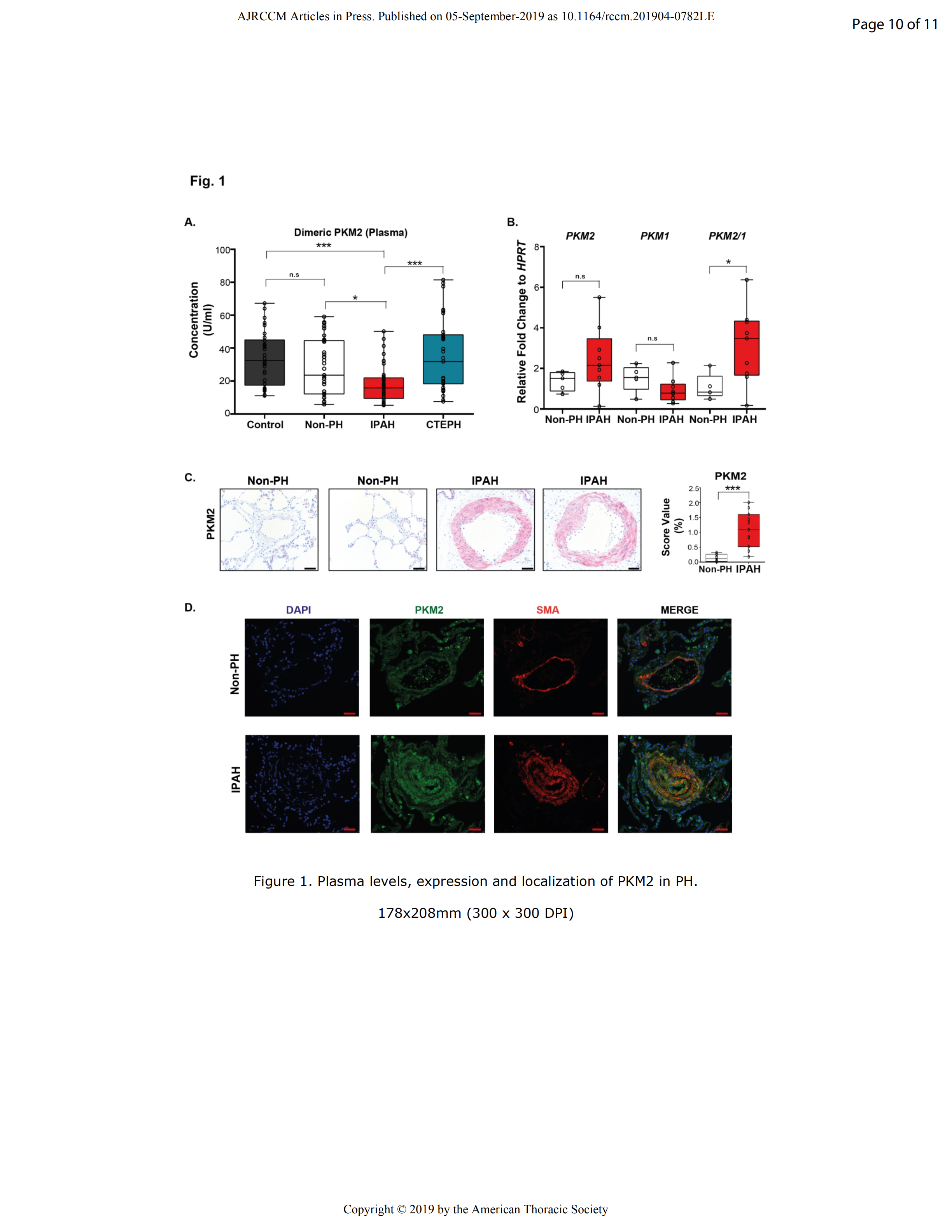
图1. PH中PKM2的血浆水平、表达以及定位。 A、采用Tu-M2PK ELISA试剂盒测定健康志愿者外周血静脉血和非PH值对照组和PH值患者中心静脉血(右心导管术)中的PKM2水平。ROC曲线下面积为0.69。95%置信区间为0.56-0.81;P < 0.01。B、定量逆转录酶聚合酶链反应分析IPAH患者(n=9)与非PH对照组(n=5) PASMCs中PKM1和PKM2的mRNA表达。C、免疫组织化学和光学显微镜定量IPAH患者(n=12)和非PH对照组(n=11)肺组织中的PKM2。标尺为50um。D、免疫荧光检测非PAH(非PH)志愿者或IPAH患者(每组3个受试者)肺部小肺动脉中PKM2(绿色)和SMA(红色)(α-actin, 平滑肌细胞的特定标志)。细胞核用DAPI(蓝色)染色。标尺:50μm。CTEPH:慢性血栓性肺动脉高压;DAPI:4 6-diamidino-2-phenylindole;HPRT:[医]次黄嘌呤磷酸核糖转移酶;IPAH:特发性肺动脉高压;n.s.:不重要的;PKM2:丙酮酸激酶2;SMA:α-smooth肌肉肌动蛋白。

图2. PKM2的磷酸化、低聚化和调节。A、WB检测及定量分析PASMCs(非PH对照组,n=5;IPAH患者,n=8)中 phospho-PKM2和总PKM2。B、免疫荧光检测及定量分析PASMCs中p-PKM2的免疫荧光染色和定量(phospho-PKM2[Tyr105]抗体,bs-3334R,Bioss)。C、WB检测及定量分析非PH对照组(n=4)及IPAH患者(n=4)肺组织及PASMCs中PKM2寡聚化(在戊二醛[0.01%]交联后)。D,WB检测非PH对照组及IPAH患者细胞核和细胞质中phospho-PKM2和总PKM2(phospho-PKM2[TYR105]抗体bs-3334R,Bioss)。Lamin B1和α-tubulin分别作为细胞核及细胞质的内参蛋白。E.WB检测及定量分析来自非PH对照组志愿者PASMCs(暴露在缺氧环境和PDGF-BB24小时后)细胞核中phospho-PKM2和总PKM2水平。F.核p-PKM2与CyclinE和PCNA的相关性分别为r=0.97,r=0.96,*P<0.05。在逐渐增加FBS含量培养条件下非PH对照组志愿者PASMCs细胞核中p-PKM 2,总PKM 2,Cyclin E和PCNA的WB检测。G.通过免疫荧光定量检测 Ki67阳性确定细胞增殖潜能,结果显示IPAH患者肺组织PASMCs增殖潜能与四聚体比率无显著相关性(r=-0.48)。P<0.05被认为具有统计学意义。Ki67抗体和肌动蛋白(SMA)α(α-actin,一种平滑肌细胞的特定标记物)。人PASMCs(传代5~7)在37℃培养24h至80%。用于刺激研究的细胞用60mm培养皿(2×105/皿)中培养,用于低聚反应的细胞用100mm培养皿(4×105/皿)。 每个培养皿的细胞)。PDGF-BB和FBS刺激前,细胞先用血清饥饿法培养24小时。缺氧环境的细胞培养在37℃缺氧环境(5%CO2和1%O2)。
作者为了了解PKM2水平升高的潜在机制,将非PH对照组的PASMCs暴露于缺氧环境和血小板衍生生长因子BB(PDGF-BB),这两种环境均可触发PASMCs细胞增殖异常。缺氧环境和PDGF-BB均显著提高PKM2 Y 105位点的磷酸化,而PDGF-BB进一步提高了核PKM2的绝对水平(图2E)。核PKM2磷酸化水平高低与细胞周期G1/S期转换的核标记物之间存在线性依赖性关系,PKM2升高与细胞增殖呈正相关(图2F)。PAH患者SMCs的增殖潜能与PKM2低聚化存在明显但非显著相关性(图2G)。PH研究中并没有涉及过PKM2的低聚化或磷酸化状态,本文关于PH内皮细胞和成纤维细胞中通过促进四聚体形成激活PKM2激活剂,逆转糖酵解表型特征并减少不同的生物合成途径的研究结果补充了这一空缺。磷酸化水平决定PKM2从高活性四聚体(葡萄糖氧化的重要因素)向低活性二聚体/单体(促进糖酵解)的转变。因此,可通过磷酸化水平依赖型的PKM2表型变化来降低PH患者肺中PK活性。IPAH患者细胞中PKM2核转录并不能排除有其他可降低血浆PKM2水平的调节机制存在的可能性。因此,PAH中的代谢重编程不仅仅是由PKM2含量的绝对升高引起,还由其变构调节以及随后的核定位引起(部分受磷酸化水平影响) 。然而,在PAH中,哪些起决定因素的分子/机制是导致PKM2二聚体分解为单体的生理机制,目前尚不清楚。
Bioss被引用产品
文中采用了Bioss公司的phospho-PKM2[TYR105]抗体(bs-3334R)对非PH对照组和IPAH患者细胞核和细胞质中p-PKM2水平,以及不同处理后非PH对照组PASMCs细胞核中p-PKM2水平进行WB检测及定量分析,使作者顺利完成了PKM2 Y105位点磷酸化水平改变酶的寡聚状态,进而影响酶的活性的验证。为作者进一步佐证Y105位点磷酸化可能促进PKM2核转录进而调节基因转录水平的观点提供了支撑。
(感谢《Am J Respir Crit Care Med》提供素材!侵删!)
Bioss相关抗体